5. Problemas resueltos
Ejercicio 1
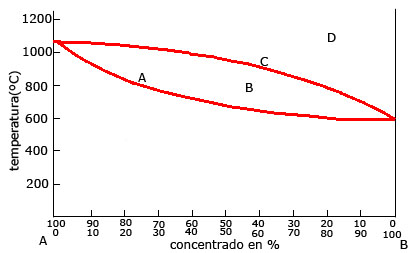
A partir del diagrama de equilibrio adjunto:
a) Indicar a que tipo de aleación corresponde, desde el punto de vista de la solubilidad.
b) Completar la tabla adjunta, indicando temperatura, concentración y cantidades en porcentaje de fases líquida y sólida en los puntos marcados.
 |
| Imagen 20. Elaboración Propia. |
Ejercicio 2
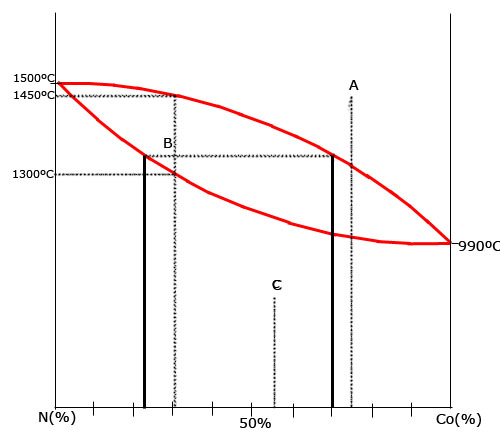
Observando el diagrama de equilibrio de fases de la aleación Ni-Cu adjunto.
 |
| Imagen 21. Elaboración Propia. |
a) Indica a que tipo de aleación corresponde, desde el punto de vista de la solubilidad.
b) Para cada punto A,B y C señalados sobre el diagrama, determina el numero de fases, su composición y la cantidad relativa de cada una de ellas.
c) indica el rango de temperaturas entre los que se produce la solidificación de la aleación correspondiente a la concentración de cada uno de los puntos A, B y C.
A partir del diagrama Cu-Ni del ejercicio anterior (que corresponde a una aleación totalmente soluble tanto en estado líquido como sólido), para una aleación que se encuentra a una temperatura de 1300ºC y tiene una concentración del 50% de Cu; determina: número de fases, composición y cantidades relativas de las fases.
Indica el rango de temperaturas en que se produce la solidificación completa de la aleación.
Ejercicio 4
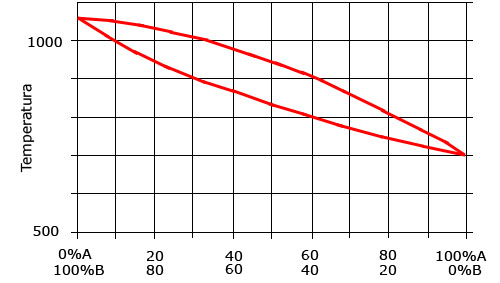
A partir del diagrama de equilibrio de una aleación de dos metales A y B de totalmente solubles tanto en estado líquido como sólido.
 |
| Imagen 22. Elaboración Propia. |
Para una aleación de concentración Co=50% de A, realiza un análisis de número de fases, concentración de las fases y cantidades relativas a las temperaturas:1000ºC, 900ºC y 800ºC.
Ejercicio 5
A partir del diagrama de equilibrio de una aleación de dos metales A y B de totalmente solubles tanto en estado líquido como sólido.
 |
| Imagen 23. Elaboración Propia. |
Una aleación de Co=40% de A, se calienta hasta que se encuentra en la zona bifásica. La composición de la fase sólida resulta ser CS=30% de A. Calcular:
a) A qué temperatura se encuentra la aleación y cuál es la composición de la fase líquida.
b) Cantidades de cada una de las fases.
Ejercicio 6
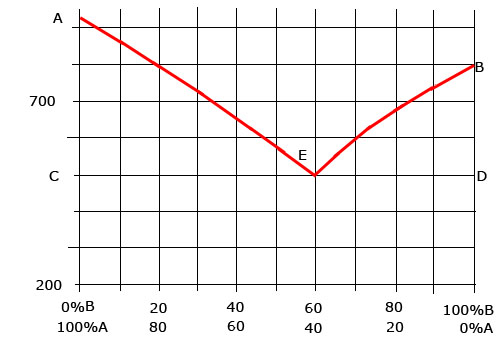
A partir del diagrama de equilibrio de fases de la aleación de dos metales A y B, totalmente solubles en estado líquido e insolubles en estados sólido y con eutéctico.
a) Indicar: zonas, puntos y líneas significativas del diagrama.
b) Para una aleación de concentración Co=40% de A, que se ha calentado hasta la zona monofásica líquido. Analizar todo lo que va ocurriendo durante el proceso de enfriamiento, suficientemente lento, hasta alcanzar la temperatura ambiente.
c) Repetir el apartado anterior para aleación de concentración Co= 80% de A y Co= 20% de A.
d) Para una aleación de Co=70% de A que se encuentra a 600ºC, determinar el número de fases y las cantidades estas que están presentes.
e) Repetir el apartado anterior si la aleación se encuentra a 300ºC.
 |
| Imagen 24. Elaboración Propia. |
Ejercicio 7
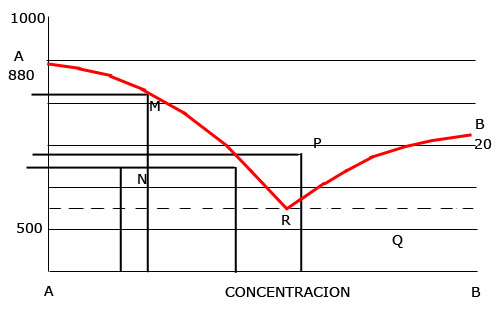
A Partir del diagrama de equilibrio de fases de una aleación de dos metales A y B, totalmente solubles en estado líquido y totalmente insolubles en estado sólido, con un eutéctico.
Observa los puntos señalados con letras mayúsculas sobre el diagrama y determina: temperaturas, concentraciones y cantidades relativas en % de cada una de las fases, de cada uno de los puntos.
 |
| Imagen 25. Elaboración Propia. |
Ejercicio 8
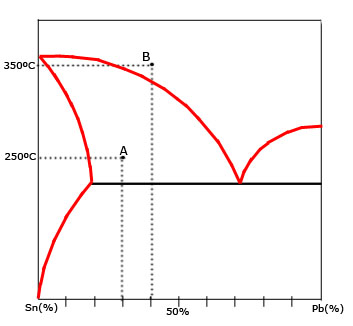
A Partir del diagrama de equilibrio de fases de la aleación de Sn y Pb, totalmente solubles en estado líquido y parcialmente insolubles en estado sólido, con un eutéctico.
a) Determina el número de fases, su composición y la cantidad relativa, en %, de cada una de ellas, para una aleación con una concentración Co=30% de Pb a una temperatura de 250ºC.
b) Repite el apartado anterior para una aleación Co=60% de Sn a 350ºC.
 |
| Imagen 26. Elaboración Propia. |
Ejercicio 9
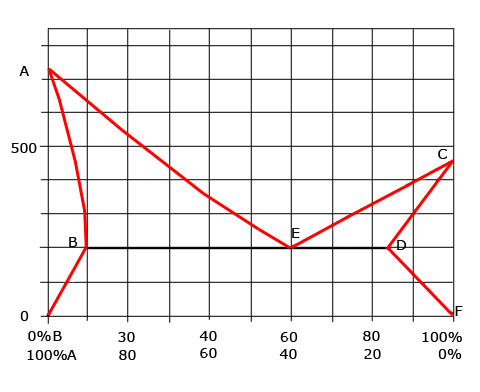
A Partir del diagrama de equilibrio de fases de la aleación de dos metales A y B, totalmente solubles en estado líquido y parcialmente insolubles en estado sólido, con un eutéctico.
a) Indicar los puntos, líneas y zonas significativas del diagrama.
Analizar el número de fases, de constituyentes, su concentración y las cantidades relativas de éstos para los siguientes puntos:
b) En el eutéctico, a
c) Para
d) Para Co=80% de A.y a una temperatura inmediatamente por encima del eutéctico 200ºC+ΔT.
e) Para Co=80% de A.y a una temperatura inmediatamente por debajo del eutéctico 200ºC-ΔT.
f) Para
 |
| Imagen 27. Elaboración Propia. |
Ejercicio 10
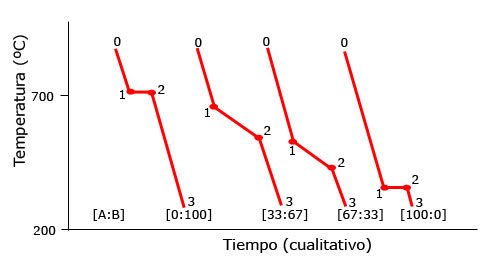
A partir de las curvas de enfriamiento adjuntas, que pertenecen a la aleación de dos metales A y B.
a) Indica a que tipo de aleación corresponde, razonando la respuesta.
b) Dibuja el diagrama de equilibrio de fases correspondiente.
 |
| Imagen 28. Elaboración Propia. |